En s’appuyant sur les données de mortalité par classe d’âge ainsi que sur les résultats de 22 études portant sur la séroprévalence, c’est-à-dire la recherche, dans des prélèvements sanguins, d’anticorps dirigés contre le SARS-CoV-2 (ce qui témoigne d’une infection par ce coronavirus), des chercheurs de l’Université de Cambridge et de l’Institut Pasteur ont estimé, dans 45 pays, le pourcentage de la population ayant été infectée au 1er septembre 2020.
Dans l’ensemble, cette analyse confirme que l’immunité collective sans vaccin reste un objectif très difficilement réalisable. Autrement dit, en attendant un vaccin, nous n’avons guère d’autre choix que de continuer de porter le masque, de nous tenir à distance les uns des autres dans les lieux publics, d’aérer les lieux clos et de respecter les mesures d’hygiène si nous voulons freiner la progression du coronavirus. Voici ce que nous apprennent ces travaux.
Des comparaisons délicates de l’incidence du Covid-19 entre pays
Pour évaluer la dynamique et la sévérité d’une épidémie, divers indicateurs sont disponibles : le nombre de cas d’infections, le nombre de décès, le taux de reproduction de base (nombre moyen de personnes infectées par une personne contaminée par le virus), le temps de doublement des cas (durée nécessaire pour que le nombre de personnes infectées double), le taux d’occupation hospitalière…
Cette multiplicité d’indicateurs implique que la comparaison des situations entre différents pays peut s’avérer un exercice périlleux, pour plusieurs raisons. Tout d’abord, les profils des populations (âge, sexe, comorbidités…) sont hétérogènes. Ensuite, tous les pays ne sont pas égaux en matière de capacités de test et de surveillance, ce qui peut rendre difficile l’estimation du nombre de cas. Enfin, la définition de ce qu’est un cas d’infection peut aussi varier d’un pays à l’autre, selon par exemple que l’on se base pour cela sur la réalisation d’un seul test RT-PCR ou de deux tests successifs, que l’on prend en compte les symptômes cliniques via une radio pulmonaire, etc.
De ce fait, les données de mortalité basées sur les certificats de décès sont souvent considérées comme un indicateur plus fiable, même si l’attribution des causes de décès peut également varier selon le pays considéré. En se basant sur ces données, les auteurs de ces travaux ont montré qu’elles peuvent être utilisées en combinaison avec le taux de létalité due à l’infection (Infection-to-Fatality Ratio ou IFR en anglais, autrement dit le rapport du nombre de décès sur le nombre de personnes infectées) pour estimer le nombre total d’infections par le SARS-CoV-2 Ce nombre est plus important que le nombre de cas détectés, qui dépend des tests.
En croisant ces données avec les résultats des enquêtes de séroprévalence, les auteurs ont aussi pu estimer les IFR par âge et par localisation. Ce point est important, car se borner à comparer la mortalité entre différents pays sans prendre en compte la structure d’âge de la population peut fournir une représentation trompeuse du niveau de transmission du SARS-CoV-2.
Des données de mortalité plus fiables chez les moins de 65 ans
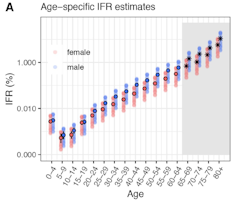
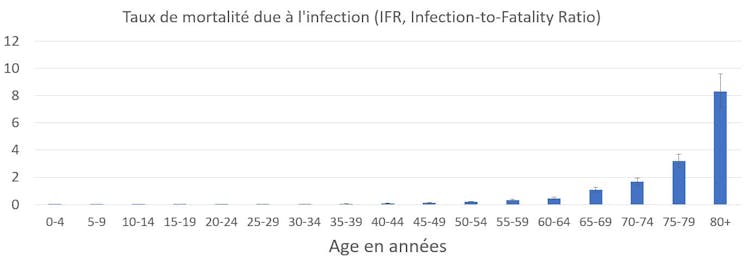
Les auteurs de ces travaux ont constaté que la létalité la plus faible concernait les 5-9 ans (IFR de 0,001 %). Pour les personnes âgées de 30 à 65 ans, le risque relatif de décès augmentait avec l’âge selon une relation log-linéaire (qui suit un modèle de régression de Poisson). Au-delà de 65 ans, le risque de létalité était beaucoup plus variable, même si l’on constate une augmentation (chez les personnes âgées de 80 ans et plus, l’IFR est de 8,29 % en moyenne pour les deux sexes).
Il faut toutefois souligner que les données concernant les personnes de plus de 65 ans pourraient être moins fiables, et les chiffres de mortalité sous-estimés, en raison du problème de notification des décès dans les maisons médicales et de retraites. Ainsi, au Royaume-Uni, au Canada et en Suède, la Covid-19 a infecté toujours de façon importante les résidents des maisons de retraite avec 20 % de décès. En effet, une fois que le virus a pénétré dans un Ehpad, il peut s’y propager rapidement au sein d’une population fragile. En revanche, certains pays d’Asie et d’Amérique du Sud ont signalé beaucoup moins de décès par Covid-19 chez les personnes âgées que prévu. Les auteurs estiment que dans certains pays cela témoigne de la réussite des politiques de protection des personnes âgées alors que pour d’autres pays (Équateur, par exemple), ces chiffres pourraient être liés à des erreurs.
Ces travaux ont également mis en évidence un risque de décès significativement plus élevé chez les hommes que chez les femmes, en particulier chez les personnes d’âge avancé : chez les 80 ans et plus, l’IFR pour les hommes est de 10,8 % tandis que celui des femmes est de 5,6 %.
Seule une petite partie des populations présente des anticorps
Cet IFR a permis aux chercheurs de mettre au point un modèle mathématique afin d’estimer quelle fraction de la population était susceptible d’avoir développé des anticorps contre le coronavirus SARS-CoV-2, en prenant en compte l’âge, le sexe, la sensibilité et la spécificité des tests au 1er septembre 2020.
Les résultats obtenus varient de 0,06 % en Corée du Sud à 62,44 % au Pérou. La modélisation globale montre que les pays d’Amérique latine ont été fortement touchés par l’épidémie : la séroconversion estimée est particulièrement importante au Pérou (62,44 %), au Mexique (45,6 %), et en Équateur (44,7 %). Cependant, les niveaux d’incertitude des estimations sont élevés pour ces pays, ce qui reflète les incertitudes des enquêtes de séroprévalences individuelles infra-nationales.
À l’inverse, les pays d’Asie du Sud semblent avoir subi beaucoup moins d’infections. C’est par exemple le cas du Japon (0,1 %), de la Chine (0,09 %) et de la Thaïlande (0,08 %). Une autre étude publiée dans Bulletin of the World Health Organization a obtenu des estimations similaires de séroprévalence : celles-ci variaient de 0,02 % à Shijiazhuang, en Chine, à 58,4 % dans les bidonvilles indiens.
Soulignons ici qu’il reste encore de nombreuses questions sur la durée et la forme de la réponse immunitaire (anticorps et réponse lymphocytaire) à l’infection par ce coronavirus, et que la présence d’anticorps n’est pas forcément synonyme de neutralisation du SARS-CoV-2nbsp;. Les anticorps neutralisants doivent spécifiquement être dirigés contre sa protéine spike S, qui lui sert de « clé » pour entrer dans les cellules.
Pour cette raison, bien que récemment plusieurs plusieurs études récentes suggèrent que certains anticorps contre le SARS-CoV-2 pourraient persister jusqu’à 5 mois dans l’organisme (avec toutefois un déclin au cours du temps), il faut rester prudent sur leur interprétation.
En outre, la réponse immunitaire a surtout été étudiée chez les patients hospitalisés ; les connaissances sont beaucoup plus faibles pour les cas asymptomatiques. Par ailleurs, quelques rares cas de ré-infections chez de jeunes patients ont été rapportés dans la littérature en Belgique, aux États-Unis, en Équateur ou à Hongkong.
La situation en France
Dans notre pays, les auteurs estiment qu’en moyenne de 3,38 % à 4,63 % de la population générale possède des anticorps anti-SARS-CoV-2. Dans les Ehpad, 7,28 % de la population aurait été infectée, ce qui s’explique par le fait que le taux d’attaque (la vitesse d’accumulation de nouveaux cas) était 1,7 fois plus élevé qu’en population générale.
Ces résultats sont cohérents avec les données de l’enquête EpiCoV, basée sur les analyses sérologiques de 12 000 participants. Ceux-ci montrent qu’en mai-juin, la séroprévalence était de 4,5 % en France. Le Haut-Rhin et Paris concentraient les taux les plus importants de personnes testées positives (respectivement 10,8 % et 9 %), tandis que les taux les plus faibles ont été relevés en Occitanie ou en Normandie (1,9 %).
Une autre enquête, SAPRIS, a porté sur trois cohortes en population générale (Constances, E3N-E4N, NutriNet-Santé et Elfe-Epipage2), totalisant 14 600 résultats sérologiques. Selon ses résultats, la proportion d’habitants des régions Grand-Est, Île-de-France et Nouvelle-Aquitaine possédant des anticorps anti-SARS-CoV-2 est respectivement de 9 %, 10 % et 3,1 % (ce qui est cohérent, la région Nouvelle-Aquitaine ayant été moins touchée par la première vague).
Les limites de ces données de mortalité et d’enquêtes de séroprévalence
L’utilisation de telles données par pays présente quelques limites. On sait notamment qu’il existe une importante variabilité au sein d’un pays en termes de transmission de l’infection, comme l’ont montré les situations des diverses régions françaises durant la première vague.
Il peut également y avoir des personnes qui ne se séroconvertissent jamais, ou qui développent uniquement une réponse impliquant des lymphocytes T, et qui seront « manqués » par les tests sérologiques. Par ailleurs, certains cas asymptomatiques peuvent avoir leur niveau d’anticorps qui diminue rapidement au cours du temps.
Un autre point limitant concerne l’attribution des causes de décès. Il peut s’avérer difficile de distinguer les patients décédés des suites directes d’une infection par le coronavirus SARS-CoV-2, et les décès associés, dus par exemple à un manque d’accès aux interventions médicales ou aux traitements (dans le cas de patients asthmatiques ou diabétiques par exemple).
Une Covid-19 non diagnostiquée peut aussi aboutir à l’exacerbation d’une maladie préexistante, ce qui peut entraîner un décès prématuré. Les retards dans le diagnostic et le traitement de divers types de cancer, par exemple, peuvent permettre la progression du cancer et affecter la survie des patients. Autre exemple : la peur de l’exposition au virus a empêché de nombreux patients atteints de problèmes cardiaques de se rendre à l’hôpital, les exposant à un risque accru de complications à long terme d’infarctus du myocarde.
Pour tenir compte de ces cas indirects, la surmortalité – l’excès de décès par rapport à la normale – constitue un bon indicateur. Elle est calculée en comparant les décès hebdomadaires de l’année en cours à une « valeur attendue » fondée sur la moyenne des cinq années précédentes. De cette façon, il est possible d’englober la mortalité indirecte due au Covid-19.
Enfin, dernier point limitant dans l’utilisation des données de mortalité et de séroprévalence : dans certains pays où les tests ont manqué et dont le système de surveillance est insuffisamment développé, il peut être difficile de se faire une idée précise de la situation. Les auteurs des travaux publiés dans la revue Nature soulignent par exemple qu’il a été estimé que, pour 6 des pays inclus dans leur analyse, les décès dus à la Covid-19 ont pu être sous-évalués (jusqu’à 40 %) ou surévalués (jusqu’à 10 %). Pour cette raison, certains spécialistes estiment que, quand le système de soins de santé a dépassé ses capacités, tous les décès peuvent être attribués, d’une manière ou d’une autre, à la pandémie.
Toutefois, malgré ces incertitudes sur le nombre de décès, ces travaux démontrent qu’il est possible d’obtenir des estimations robustes à partir des données de séroprévalence à l’échelle mondiale. Cette approche peut s’avérer utile pour les pays ou les régions qui n’ont pas les moyens de mettre en place une enquête de séroprévalence.